Biotecnología
Un nuevo modelo proporciona una ventana sin precedentes al desarrollo embrionario humano
Crea estructuras que imitan al embrión humano y sus tejidos de soporte a partir de células madre
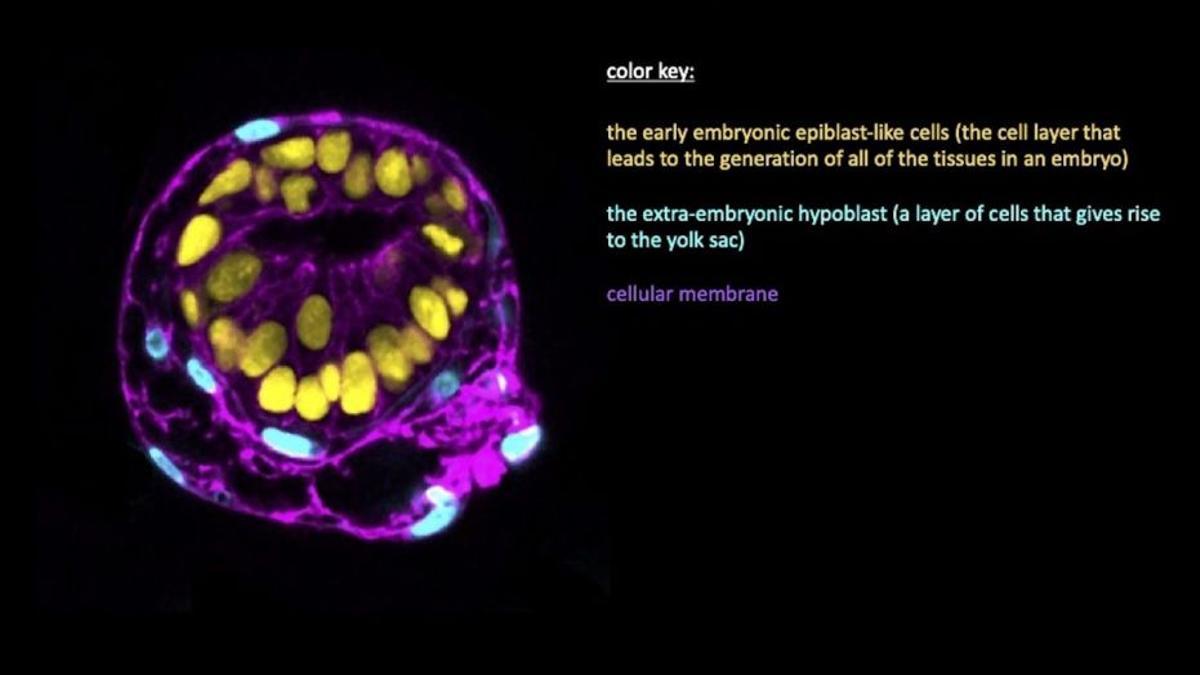
Imagen microscópica del modelo de embrión humano. / Monique Pedroza et al.
El desarrollo embrionario humano es difícil de estudiar por razones éticas y técnicas. Un nuevo modelo incluye componentes embrionarios y extraembrionarios que interactúan durante la gastrulación, el momento clave en el que se forman los ejes corporales y las capas germinales. El modelo ofrece nuevas posibilidades para investigar el desarrollo humano y sus enfermedades.
El desarrollo embrionario humano es uno de los procesos más fascinantes y misteriosos de la biología.
En pocas semanas, una única célula se transforma en un organismo complejo con millones de células especializadas y organizadas en tejidos y órganos.
Sin embargo, estudiar este proceso en el contexto humano plantea importantes desafíos éticos y técnicos, ya que implica el uso de embriones humanos.
Modelos alternativos
Para superar estos obstáculos, los científicos han recurrido a modelos alternativos basados en células madre, que pueden generar estructuras similares a las de los embriones humanos en el laboratorio.
Estos modelos han permitido avanzar en el conocimiento de las primeras etapas del desarrollo humano, pero tienen limitaciones. Por ejemplo, la mayoría de ellos carecen de los tejidos que rodean y sostienen al embrión, que son esenciales para su crecimiento y supervivencia.
Nuevo modelo
Un nuevo modelo desarrollado por investigadores de la Universidad de Yale ofrece una ventana sin precedentes al desarrollo embrionario humano al incluir tanto componentes embrionarios como extraembrionarios, según sus creadores.
Este modelo permitirá estudiar cómo estas dos partes interactúan alrededor de las etapas de la gastrulación, que es el momento crítico en el que las células embrionarias se especializan y empiezan a formar los ejes corporales. El modelo también ofrecerá potenciales nuevos pistas sobre por qué los embarazos pueden fallar o sobre los orígenes de los trastornos congénitos.
El equipo, liderado por Berna Sozen y Zachary Smith, ambos profesores asistentes de genética en la Facultad de Medicina de Yale, han publicado sus hallazgos en la revista Nature.
Células madre pluripotentes
El equipo utilizó células madre pluripotentes inducidas (iPSC), que son células adultas reprogramadas para volver a un estado similar al embrionario, capaces de generar cualquier tipo de célula del cuerpo.
A partir de estas células, los investigadores generaron estructuras tridimensionales llamadas gastruloides, que imitan algunos aspectos del embrión humano durante la gastrulación, que comienza dos a tres semanas después de la concepción.
Los gastruloides se cultivaron junto con estructuras extraembrionarias derivadas también de iPSC, como el saco vitelino y el trofoblasto.
Estas estructuras proporcionan nutrientes y señales al embrión y son imprescindibles para su implantación y desarrollo. Al combinar ambos componentes, los investigadores lograron crear lo que califican como un modelo más completo y realista del desarrollo embrionario humano.
Ventajas comparativas
El modelo tiene varias ventajas frente a otros modelos existentes, explican los investigadores. Por ejemplo, permite observar la formación de los ejes corporales anteroposterior (cabeza-cola) y dorsoventral (espalda-vientre) del embrión humano, así como la aparición de las tres capas germinales (ectodermo, mesodermo y endodermo) que darán lugar a los diferentes tejidos y órganos del cuerpo.
Además, el modelo tiene una duración limitada (unos 12 días), lo que evita posibles problemas éticos relacionados con el potencial desarrollo del sistema nervioso.
En muchos países, la investigación con embriones humanos está restringida por la llamada regla de los 14 días, que prohíbe cultivar o experimentar con embriones humanos más allá de ese límite temporal. El nuevo desarrollo está instalado en un margen cómodo desde el punto de vista legal y ético.
No propiamente humano
El estudio publicado ahora concluye que este modelo representa una herramienta innovadora para estudiar el desarrollo embrionario humano en un contexto más fisiológico y relevante.
Aclara también que este modelo carece de células trofoectodérmicas, que son necesarias para que un embrión se implante en el útero. Sozen dice al respecto en un comunicado que este modelo no puede crecer más ni implantarse y que, por lo tanto, no se considera un embrión propiamente humano.
El modelo también abre nuevas posibilidades para investigar las bases moleculares y celulares del desarrollo humano, así como para explorar las causas y posibles tratamientos de las enfermedades relacionadas con el desarrollo.
Suma y sigue
Este nuevo modelo se suma al menos a otros tres anteriores, de los que informamos en otro artículo, y refleja la competición que se ha desatado entre diversos laboratorios sobre un tema a la vez interesante y sensible.
Todos podrían facilitar el estudio de las etapas más desconocidas y complejas de la formación del embrión humano, pero también plantean cuestiones éticas y legales sobre su estatus y regulación que siguen sin resolverse.
Referencia
Self-patterning of human stem cells into post-implantation lineages. Monique Pedroza et al. Nature (2023). DOI:https://doi.org/10.1038/s41586-023-06354-4
- Una enorme plataforma de hielo antártica salta cada día e intriga a los expertos
- Los taxis aéreos recorrerán los cielos de París durante los juegos olímpicos de 2024
- Descubren una nueva forma de vida nacida de la fusión de una bacteria y un alga
- Detectan "arañas negras" en la misteriosa "Ciudad Inca" de Marte
- La microbiota intestinal puede modificarse mediante una herida
- Una extraña y antigua megaestructura acecha bajo el mar Báltico
- Descubren una "segunda luna" orbitando la Tierra y determinan su origen
- La memoria “daña” al cerebro a largo plazo
